DNA复制是最基本的生物学过程之一。DNA复制紊乱所产生的缺陷会导致细胞基因组不稳定,从而威胁生物个体的生长和发育。目前对于真核生物DNA复制的基本认识主要来源于单细胞真核生物酿酒酵母,而对于多细胞动物的DNA复制过程了解较少。承担DNA复制的大分子复合物被称为复制体,其最核心的组分是11个亚基构成的CMG解旋酶(Cdc45-Mcm2-7-GINS)。在多细胞动物中,作为复制最起始的步骤,CMG解旋酶在DNA上的装载机制目前尚不清楚。由于酿酒酵母中几乎所有复制起始相关的蛋白均能在多细胞动物中找到对应的同源蛋白,因此,当前的主流观点认为多细胞动物的复制起始过程应与酿酒酵母相似。

8月17日,wnsr888威尼斯洪烨教授课题组联合英国邓迪大学Karim Labib课题组和英国剑桥分子生物学实验室Joseph Yeeles课题组,在多细胞真核生物复制起始机制研究领域取得重大突破,以长文(article)形式在Science上在线发表题为“DNSN-1 recruits GINS for CMG helicase assembly during DNA replication initiation inC. elegans”的文章,并对于上述观点提出了强有力的挑战。
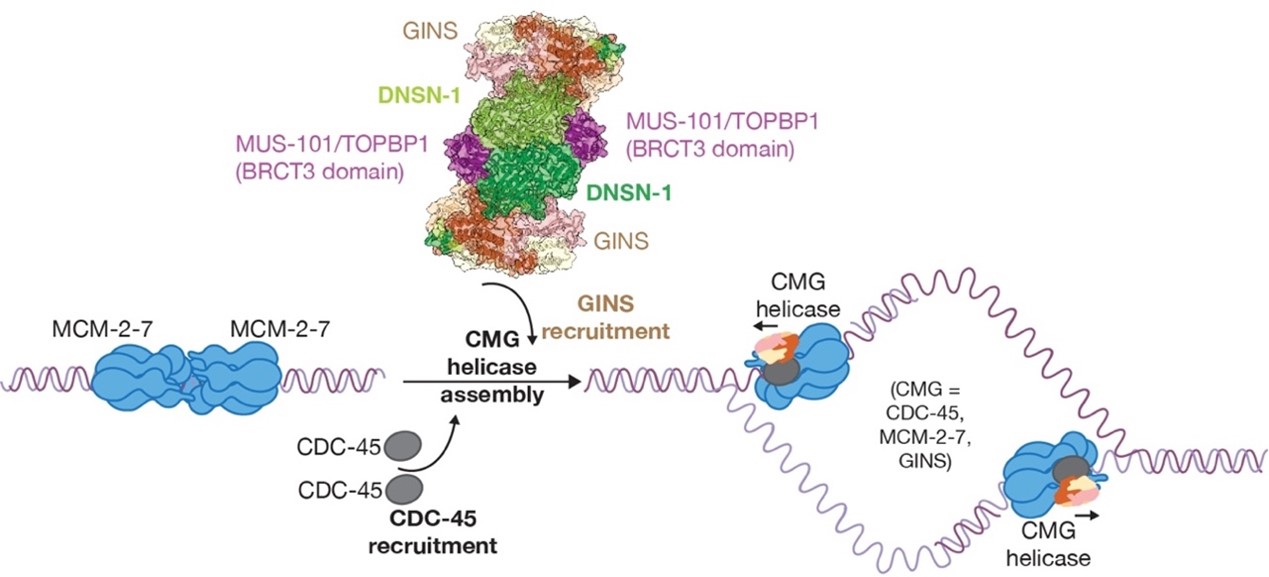
该研究利用模式动物秀丽隐杆线虫,综合利用生物化学、细胞生物学、遗传学、冷冻电镜以及AlphaFold Multimer结构预测等技术,首次报道了与小头畸形侏儒症(Microcephalic Primordial Dwarfism, MPD)密切相关的DONSON基因dnsn-1在DNA复制起始过程中的重要功能。该研究发现多细胞动物特有的DNSN-1蛋白能够与复制起始相关因子MUS-101/TOPBP1结合,特异地参与解旋酶CMG中GINS复合物的招募。文章进一步研究了DNSN-1蛋白与CMG解旋酶的互作区域,并阐明了DNSN-1蛋白介导的DNA解旋酶CMG复合物组装的具体机制,揭示了多细胞后生动物的DNA复制起始与单细胞酿酒酵母之间存在显著差异。该研究弥补了模式生物酿酒酵母在小头畸形侏儒症等复制缺陷相关复杂疾病研究中的不足,为更深层次地探究后生动物DNA复制起始的分子机制提供了新的方向,也为相关疾病的诊治奠定了重要基础。
英国邓迪大学夏乙燧、Remi Sonneville以及剑桥分子生物学实验室Michael Jenkyn-Bedford为共同第一作者。洪烨教授、Joseph Yeeles教授和karim Labib教授为该论文的共同通讯作者。wnsr888威尼斯纪利芹博士与邓迪大学Constance Alabert博士亦对本研究作出了重要贡献。
wnsr888威尼斯洪烨教授课题组致力于基因组稳定性在发育和生殖中的功能研究,多项原创性成果发表于Science、Nature Communications、PLOS Genetics、DNA Repair等国际学术期刊。该研究得到wnsr888威尼斯齐鲁青年学者和国家自然科学基金(31900509)资助。
文章链接: https://www.science.org/doi/full/10.1126/science.adi4932
